Danes poznan koncept PRP se je na področju hematologije prvič pojavil v sedemdesetih letih prejšnjega stoletja.Hematologi so pred desetletji ustvarili izraz PRP, da bi opisali plazmo, pridobljeno iz števila trombocitov, ki je višje od osnovne vrednosti periferne krvi.Več kot deset let kasneje je bil PRP uporabljen v maksilofacialni kirurgiji kot oblika fibrina, bogatega s trombociti (PRF).Vsebnost fibrina v tem derivatu PRP ima pomembno vrednost zaradi njegove adhezivnosti in lastnosti v stanju dinamičnega ravnovesja, medtem ko ima PRP trajne protivnetne lastnosti in spodbuja celično proliferacijo.Končno je okoli devetdesetih let prejšnjega stoletja PRP postal priljubljen.Končno se je ta tehnologija prenesla na druga medicinska področja.Od takrat je bila tovrstna pozitivna biologija obsežno raziskana in uporabljena pri zdravljenju različnih mišično-skeletnih poškodb profesionalnih športnikov, kar je dodatno spodbudilo njeno široko pozornost v medijih.Poleg učinkovitosti v ortopediji in športni medicini se PRP uporablja tudi v oftalmologiji, ginekologiji, urologiji in kardiologiji, pediatriji in plastični kirurgiji.V zadnjih letih so PRP hvalili tudi dermatologi zaradi njegovega potenciala pri zdravljenju kožnih razjed, popravljanju brazgotin, regeneraciji tkiva, pomlajevanju kože in celo izpadanju las.
Glede na to, da lahko PRP neposredno manipulira s celjenjem in vnetnimi procesi, je treba kot referenco uvesti zdravilno kaskado.Proces celjenja je razdeljen na naslednje štiri stopnje: hemostaza;vnetje;Proliferacija celic in matriksa ter končno preoblikovanje rane.
Zdravljenje tkiv
Aktivira se kaskadna reakcija celjenja tkiva, kar vodi do agregacije trombocitov, nastajanja strdkov in razvoja začasnega zunajceličnega matriksa (ECM).Nato se trombociti oprimejo izpostavljenega kolagena in proteina ECM, kar sproži sproščanje bioaktivnih molekul, prisotnih v a-granulah.Trombociti vsebujejo različne bioaktivne molekule, vključno z rastnimi faktorji, kemoterapevtskimi faktorji in citokini, pa tudi vnetne mediatorje, kot so prostaglandin, prostata ciklin, histamin, tromboksan, serotonin in bradikinin.
Končna faza celjenja je odvisna od preoblikovanja rane.Preoblikovanje tkiva je strogo regulirano, da se vzpostavi ravnovesje med anabolnimi in katabolnimi reakcijami.Na tej stopnji trombocitni rastni faktor (PDGF) in transformirajoči rastni faktor (TGF- β) fibronektin in fibronektin spodbujata proliferacijo in migracijo fibroblastov ter sintezo komponent ECM.Vendar je čas zorenja rane v veliki meri odvisen od resnosti rane, individualnih značilnosti in specifične sposobnosti celjenja poškodovanega tkiva.Nekateri patofiziološki in presnovni dejavniki lahko vplivajo na proces celjenja, kot so ishemija tkiva, hipoksija, okužba, neravnovesje rastnega faktorja in celo bolezni, povezane z metaboličnim sindromom.
Provnetno mikrookolje ovira proces celjenja.Bolj zapleteno je, da visoka aktivnost proteaze zavira naravno delovanje rastnega faktorja (GF).Poleg mitotičnih, angiogenih in kemotaktičnih lastnosti je PRP tudi bogat vir številnih rastnih faktorjev.Te biomolekule lahko preprečijo škodljive učinke v vnetnih tkivih z nadzorom povečanega vnetja in vzpostavitvijo anaboličnih dražljajev.Ob upoštevanju teh značilnosti lahko raziskovalci najdejo velik potencial pri zdravljenju različnih kompleksnih poškodb.
Številne bolezni, zlasti tiste mišično-skeletne narave, so močno odvisne od bioloških pripravkov, ki uravnavajo vnetni proces, kot je PRP za zdravljenje osteoartritisa.V tem primeru je zdravje sklepnega hrustanca odvisno od natančnega ravnovesja anaboličnih in katabolnih reakcij.Ob upoštevanju tega načela se lahko uporaba nekaterih pozitivnih bioloških učinkovin izkaže za uspešno pri doseganju zdravega ravnovesja.PRP, ker sprošča trombocite α- Rastni faktorji, ki jih vsebujejo zrnca, se pogosto uporabljajo za uravnavanje potenciala tkivne transformacije, kar tudi zmanjšuje bolečino.Pravzaprav je eden glavnih ciljev zdravljenja s PRP zaustavitev glavnega vnetnega in katabolnega mikrookolja ter spodbujanje preobrazbe v protivnetna zdravila.Drugi avtorji so že dokazali, da PRP, aktiviran s trombinom, poveča sproščanje več bioloških molekul.Ti dejavniki vključujejo rastni faktor hepatocitov (HGF) in faktor tumorske nekroze (TNF-α), transformacijski rastni faktor beta1 (TGF-β1), vaskularni endotelijski rastni faktor (VEGF) in rastni faktor epidermisa (EGF).Druge študije so pokazale, da PRP spodbuja zvišanje ravni mRNA kolagena tipa ii in agrekana, hkrati pa zmanjša zaviranje provnetnega citokina interlevkina – (IL) 1 na njih.Predlagano je bilo tudi, da lahko PRP zaradi HGF in TNF-α [28] pomaga vzpostaviti protivnetni učinek.Oba molekularna pripravka zmanjšata aktivnost in ekspresijo jedrnega faktorja kappaB (NF-κВ);Drugič, ekspresija TGF- β 1 preprečuje tudi kemotakso monocitov in s tem preprečuje učinek TNF- α na transaktivacijo kemokinov.Zdi se, da igra HGF nepogrešljivo vlogo pri protivnetnem učinku, ki ga povzroči PRP.Ta močan protivnetni citokin uniči signalno pot NF-κ B in ekspresija vnetnih citokinov zavira vnetni odziv.Poleg tega lahko PRP zmanjša tudi visoko raven dušikovega oksida (NO).Na primer, dokazano je, da povečanje koncentracije NO v sklepnem hrustancu zavira sintezo kolagena in inducira apoptozo hondrocitov, hkrati pa povečuje sintezo matričnih metaloproteinaz (MMP), s čimer spodbuja transformacijo katabolizma.Kar zadeva celično degeneracijo, velja tudi, da PRP lahko manipulira z avtofagijo določenih vrst celic.Ko dosežejo končno stanje staranja, nekatere celične skupine izgubijo potencial statičnega stanja in samoobnavljanja.Vendar so nedavne študije pokazale, da lahko zdravljenje s PRP dobro odpravi ta škodljiva stanja.Moussa in sodelavci so dokazali, da lahko PRP inducira zaščito hondrocitov s povečanjem avtofagije in protivnetnih markerjev, hkrati pa zmanjša apoptozo hrustanca človeškega osteoartritisa.Garcia Pratt idr.Poroča se, da avtofagija določa prehod med mirovanjem in staranjem mišičnih matičnih celic.Raziskovalci verjamejo, da in vivo normalizacija integrirane avtofagije preprečuje kopičenje znotrajcelične poškodbe in preprečuje staranje in funkcionalni upad satelitskih celic.Celo pri staranju človeških matičnih celic, kot je nedavno, sta Parrish in Rodes prav tako pomembno prispevala, kar je dodatno razkrilo protivnetni potencial PRP.Tokrat je poudarek na interakciji med trombociti in nevtrofilci.V svoji preiskavi so raziskovalci pojasnili, da so aktivirane trombocite, ki jih sprosti arahidonska kislina, absorbirali nevtrofilci in jih pretvorili v levkotriene in prostaglandine, ki so znane vnetne molekule.Vendar pa interakcija trombocitnih nevtrofilcev omogoča pretvorbo levkotriena v lipoproteine, za katere se je izkazalo, da so učinkoviti protivnetni proteini, ki lahko omejijo aktivacijo nevtrofilcev in preprečijo dializo ter spodbujajo dedovanje do končne stopnje zdravilne kaskade.
Provnetno mikrookolje ovira proces celjenja.Bolj zapleteno je, da visoka aktivnost proteaze zavira naravno delovanje rastnega faktorja (GF).Poleg mitotičnih, angiogenih in kemotaktičnih lastnosti je PRP tudi bogat vir številnih rastnih faktorjev.Te biomolekule lahko preprečijo škodljive učinke v vnetnih tkivih z nadzorom povečanega vnetja in vzpostavitvijo anabolične stimulacije.
Celični faktor
Citokini v PRP igrajo ključno vlogo pri manipulaciji procesa obnavljanja tkiva in uravnavanju vnetnih poškodb.Protivnetni citokini so širok spekter biokemičnih molekul, ki posredujejo pri odzivu proinflamatornih citokinov, ki ga večinoma inducirajo aktivirani makrofagi.Protivnetni citokini medsebojno delujejo s specifičnimi zaviralci citokinov in topnimi citokinskimi receptorji za uravnavanje vnetja.Med glavna protivnetna zdravila, citokine, uvrščamo antagoniste receptorjev za interlevkin (IL) – 1, IL-4, IL-10, IL-11 in IL-13.Glede na različne vrste ran so nekateri citokini, kot so interferon, faktor zaviranja levkemije, TGF-β in IL-6, ki lahko kažejo proinflamatorne ali protivnetne učinke.TNF-α、 IL-1 in IL-18 imata določene citokinske receptorje, ki lahko zavirajo proinflamatorni učinek drugih proteinov [37].IL-10 je eden najučinkovitejših protivnetnih citokinov, ki lahko zniža proinflamatorne citokine, kot so IL-1, IL-6 in TNF-α, in poveča protivnetne dejavnike.Ti protiregulacijski mehanizmi igrajo ključno vlogo pri proizvodnji in delovanju vnetnih citokinov.Poleg tega lahko nekateri citokini sprožijo specifične signalne odzive za stimulacijo fibroblastov, ki so kritični za obnovo tkiva.Vnetni citokin TGF β 1、IL-1 β、 IL-6, IL-13 in IL-33 stimulira fibroblaste, da se diferencirajo v miofibroblaste in izboljšajo ECM [38].Po drugi strani fibroblasti izločajo citokin TGF-β、 IL-1β、 IL-33, CXC in CC kemokini spodbujajo vnetni odziv z aktiviranjem in rekrutiranjem imunskih celic, kot so makrofagi.Te vnetne celice igrajo več vlog v rani, predvsem s spodbujanjem čiščenja rane – in biosintezo kemokinov, metabolitov in rastnih faktorjev, kar je ključnega pomena za rekonstrukcijo novih tkiv.Zato imajo citokini v PRP pomembno vlogo pri stimulaciji imunskega odziva, posredovanega s celično vrsto, in spodbujanju regresije vnetne stopnje.Pravzaprav so nekateri raziskovalci ta proces imenovali "regenerativno vnetje", kar kaže, da je vnetna stopnja kljub bolnikovi tesnobi nujen in kritičen korak za uspešen zaključek procesa popravljanja tkiva, ob upoštevanju epigenetskega mehanizma, ki ga signalizira vnetje. spodbuja plastičnost celic.
Vloga citokinov pri vnetju plodove kože je zelo pomembna za raziskave regenerativne medicine.Razlika med fetalnimi in odraslimi mehanizmi celjenja je v tem, da se poškodovana fetalna tkiva včasih povrnejo v prvotno stanje glede na fetalno starost in ustrezne vrste tkiv.Pri ljudeh se lahko fetalna koža popolnoma regenerira v 24 tednih, pri odraslih pa lahko celjenje ran povzroči nastanek brazgotin.Kot vemo, so v primerjavi z zdravimi tkivi mehanske lastnosti brazgotin znatno zmanjšane, njihove funkcije pa omejene.Posebna pozornost je namenjena citokinu IL-10, za katerega je bilo ugotovljeno, da je močno izražen v amnijski tekočini in plodovi koži ter dokazano igra vlogo pri popravljanju plodove kože brez brazgotin, kar spodbuja pleiotropni učinek citokina.ZgheibC et al.Proučevali so presaditev fetalne kože v transgenske miši z izločenim (KO) IL-10 in kontrolne miši.Miši IL-10KO so pokazale znake vnetja in nastanek brazgotin okoli presadkov, medtem ko presadki v kontrolni skupini niso pokazali pomembnih sprememb v biomehanskih lastnostih in brez celjenja brazgotin.
Pomembnost uravnavanja občutljivega ravnovesja med izražanjem protivnetnih in provnetnih citokinov je v tem, da slednji, ko so prekomerno proizvedeni, na koncu pošljejo signale celične razgradnje z zmanjšanjem izražanja določenih genov.Na primer, v mišično-skeletni medicini IL-1 β navzdol uravnava SOX9, ki je odgovoren za razvoj hrustanca.SOX9 proizvaja pomembne transkripcijske faktorje za razvoj hrustanca, uravnava kolagen tipa II alfa 1 (Col2A1) in je odgovoren za kodiranje genov kolagena tipa II.IL-1 β Končno se je zmanjšala ekspresija Col2A1 in agrekana.Vendar je bilo dokazano, da zdravljenje z izdelki, bogatimi s trombociti, zavira IL-1 β. Še vedno je izvedljiv zaveznik regenerativne medicine za ohranjanje izražanja genov, ki kodirajo kolagen, in zmanjšanje apoptoze hondrocitov, ki jo povzročajo vnetni citokini.
Anabolična stimulacija: Poleg uravnavanja vnetnega stanja poškodovanega tkiva citokini v PRP sodelujejo tudi pri anabolični reakciji, tako da igrajo svojo vlogo mitoze, kemične privlačnosti in proliferacije.To je študija in vitro, ki so jo vodili Cavallo et al.Preučiti učinke različnih PRP na človeške hondrocite.Raziskovalci so opazili, da produkti PRP z relativno nizkimi koncentracijami trombocitov in levkocitov stimulirajo normalno aktivnost hondrocitov, kar je ugodno za spodbujanje nekaterih celičnih mehanizmov anaboličnega odziva.Na primer, opazili so izražanje kolagena tipa ii in agregacijskih glikanov.Nasprotno pa se zdi, da visoke koncentracije trombocitov in levkocitov stimulirajo druge celične signalne poti, ki vključujejo različne citokine.Avtorji menijo, da je to lahko posledica prisotnosti velikega števila belih krvnih celic v tej posebni formulaciji PRP.Zdi se, da so te celice odgovorne za povečano izražanje določenih rastnih faktorjev, kot so VEGF, FGF-b in interlevkina IL-1b in IL-6, ki lahko nato stimulirajo TIMP-1 in IL-10.Z drugimi besedami, v primerjavi s "slabo" formulo PRP se zdi, da mešanica PRP, bogata s trombociti in belimi krvnimi celicami, spodbuja relativno invazivnost hondrocitov.
Študija, ki so jo zasnovali Schnabel et al.je bil zasnovan za oceno vloge avtolognih biomaterialov v tkivu konjske kite.Avtorji so zbrali vzorce krvi in tetiv šestih mladih odraslih konj (starih 2-4 let) in se osredotočili na preučevanje vzorca genske ekspresije, DNK in vsebnosti kolagena v eksplantatih tetiv flexor digitorum superficialis konj, gojenih v mediju, ki je vseboval PRP. ali drugih krvnih pripravkov.Tetivne eksplante smo gojili v krvi, plazmi, PRP, plazmi s pomanjkanjem trombocitov (PPP) ali aspiratih kostnega mozga (BMA), aminokisline pa smo dodali 100 %, 50 % ali 10 % DMEM brez seruma.Pri izvajanju uporabne biokemične analize po ... so raziskovalci ugotovili, da je bila koncentracija TGF- β PDGF-BB in PDGF-1 v mediju PRP še posebej višja kot pri vseh drugih testiranih krvnih izdelkih.Poleg tega so tkiva kit, gojena v 100 % mediju PRP, pokazala povečano gensko izražanje matričnih proteinov COL1A1, COL3A1 in COMP, vendar niso povečala katabolnih encimov MMPs3 in 13. Vsaj kar zadeva strukturo kite, ta študija in vivo podpira uporabo autolo – krvni produkt protina ali PRP za zdravljenje tendinitisa velikih sesalcev.
Chen et al.Nadalje so razpravljali o rekonstruktivnem učinku PRP.V svojih prejšnjih serijah študij so raziskovalci dokazali, da PRP poleg povečanja tvorbe hrustanca spodbuja tudi povečanje sinteze ECM in zavira vnetno reakcijo sklepnega hrustanca in jedra pulposusa.PRP lahko aktivira TGF s fosforilacijo Smad2/3- β Signalna pot ima pomembno vlogo pri rasti in diferenciaciji celic.Poleg tega se domneva tudi, da fibrinski strdki, ki nastanejo po aktivaciji PRP, zagotavljajo trdno tridimenzionalno strukturo, ki omogoča, da se celice oprimejo, kar lahko vodi do izgradnje novih tkiv.
Drugi raziskovalci so pomembno prispevali k zdravljenju kroničnih kožnih razjed na področju dermatologije.Tudi to je omembe vredno.Na primer, raziskava, ki sta jo izvedla Hessler in Shyam leta 2019, kaže, da je PRP dragocen kot izvedljivo in učinkovito alternativno zdravljenje, medtem ko kronična razjeda, odporna na zdravila, še vedno prinaša znatno ekonomsko breme za zdravstveno varstvo.Zlasti razjeda na stopalu zaradi sladkorne bolezni je dobro znana velika zdravstvena težava, zaradi katere je okončine enostavno amputirati.Študija, ki so jo objavili Ahmed et al.leta 2017 je pokazalo, da lahko avtologni PRP gel spodbudi celjenje ran pri bolnikih s kronično diabetično razjedo na stopalu s sproščanjem potrebnih rastnih faktorjev in s tem znatno izboljša hitrost celjenja.Podobno so Gonchar in sodelavci pregledali in razpravljali o regenerativnem potencialu PRP in koktajlov rastnega faktorja pri izboljšanju zdravljenja razjed na stopalih s sladkorno boleznijo.Raziskovalci so predlagali, da je uporaba mešanic rastnih faktorjev verjetno možna rešitev, ki lahko izboljša prednosti uporabe PRP in enega samega rastnega faktorja.Zato lahko v primerjavi z uporabo enega samega rastnega faktorja kombinacija PRP in drugih strategij zdravljenja znatno pospeši celjenje kroničnih razjed.
Fibrin
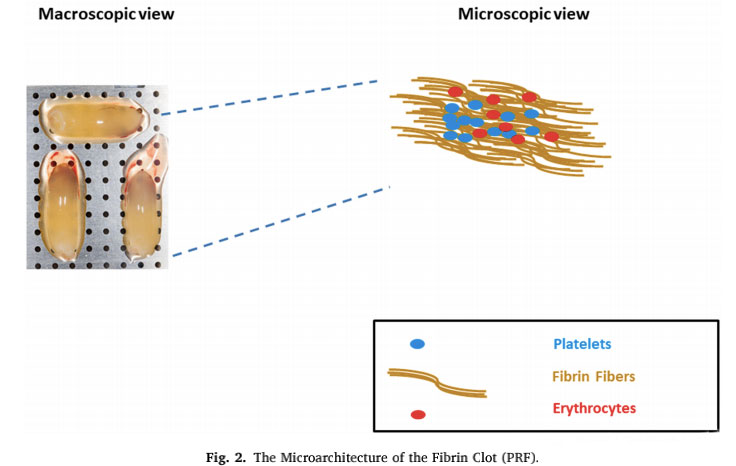
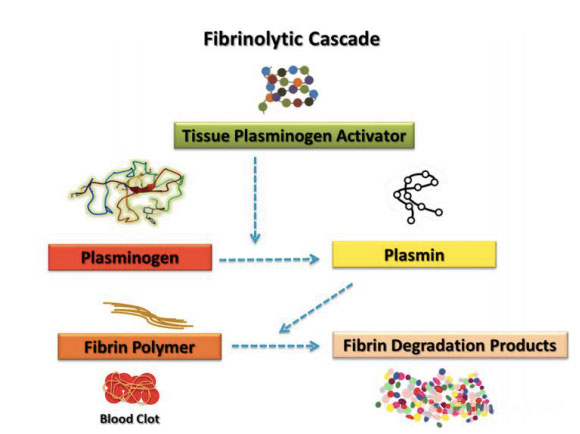
Trombociti nosijo več dejavnikov, povezanih s fibrinolitičnim sistemom, ki lahko uravnavajo fibrinolitično reakcijo navzgor ali navzdol.Časovno razmerje in relativni prispevek hematoloških komponent in funkcije trombocitov pri razgradnji strdka je še vedno problem, vreden obsežne razprave v skupnosti.Literatura uvaja številne študije, ki se osredotočajo samo na trombocite, ki so znani po svoji sposobnosti vplivanja na proces celjenja.Kljub velikemu številu izjemnih študij je bilo ugotovljeno, da tudi druge hematološke komponente, kot so koagulacijski faktorji in fibrinolitični sistemi, pomembno prispevajo k učinkovitemu celjenju ran.Po definiciji je fibrinoliza kompleksen biološki proces, ki je odvisen od aktivacije določenih encimov za spodbujanje razgradnje fibrina.Drugi avtorji so predlagali reakcijo fibrinolize, da so produkti razgradnje fibrina (fdp) dejansko lahko molekularni dejavniki, ki so odgovorni za spodbujanje popravljanja tkiva.Zaporedje pomembnih bioloških dogodkov pred tem je odlaganje fibrina in odstranitev angiogeneze, ki je potrebna za celjenje ran.Tvorba strdkov po poškodbi služi kot zaščitna plast za zaščito tkiv pred izgubo krvi in vdorom mikrobnih povzročiteljev ter zagotavlja začasno matrico, skozi katero lahko celice migrirajo med procesom popravljanja.Strdek nastane zaradi fibrinogena, ki ga cepi serinska proteaza, trombociti pa se zberejo v zamreženem fibrinskem vlaknu.Ta reakcija je sprožila polimerizacijo fibrinskega monomera, ki je glavni dogodek nastanka krvnih strdkov.Strdek lahko uporabimo tudi kot rezervoar citokinov in rastnih faktorjev, ki se sproščajo med degranulacijo aktiviranih trombocitov.Fibrinolitični sistem je strogo reguliran s plazminom in igra ključno vlogo pri pospeševanju celične migracije, biološki uporabnosti rastnih faktorjev in uravnavanju drugih proteaznih sistemov, ki sodelujejo pri vnetju in regeneraciji tkiv.Znano je, da se ključne komponente fibrinolize, kot sta receptor aktivatorja plazminogena urokinaze (uPAR) in inhibitor aktivatorja plazminogena-1 (PAI-1), izražajo v mezenhimskih izvornih celicah (MSC), ki so posebne vrste celic, potrebne za uspešno celjenje ran. .
Celična migracija
Aktivacija plazminogena prek povezave uPA uPAR je proces, ki spodbuja migracijo vnetnih celic, ker povečuje zunajcelično proteolizo.Zaradi pomanjkanja transmembranskih in intracelularnih domen potrebuje uPAR koreceptorje, kot sta integrin in vitelin, za uravnavanje celične migracije.Nadalje je pokazalo, da je vezava uPA uPAR povzročila povečanje afinitete uPAR za vitrektonektin in integrin, kar je spodbudilo celično adhezijo.Inhibitor aktivatorja plazminogena-1 (PAI-1) nato povzroči odcepitev celic.Ko se veže na uPA kompleksa upar upar integrin na celični površini, uniči interakcijo med upar vitelinom in integrin vitelinom.
V okviru regenerativne medicine se mezenhimske matične celice kostnega mozga mobilizirajo iz kostnega mozga v primeru hude poškodbe organa, zato jih lahko najdemo v obtoku bolnikov z več zlomi.Vendar pa v posebnih primerih, kot je končna odpoved ledvic, končna odpoved jeter ali med zavrnitvijo po presaditvi srca, teh celic morda ne bodo zaznali v krvi [66].Zanimivo je, da teh mezenhimskih (stromalnih) matičnih celic, pridobljenih iz človeškega kostnega mozga, ni bilo mogoče odkriti v krvi zdravih posameznikov [67].Vloga uPAR pri mobilizaciji mezenhimskih matičnih celic kostnega mozga (BMSC) je bila predlagana že prej, kar je podobno pojavu uPAR pri mobilizaciji hematopoetskih matičnih celic (HSC).Varabaneni idr.Rezultati so pokazali, da je uporaba granulocitne kolonije stimulirajočega faktorja pri miših s pomanjkanjem uPAR povzročila odpoved MSC, kar je ponovno okrepilo podporno vlogo sistema fibrinolize pri celični migraciji.Nadaljnje študije so tudi pokazale, da receptorji uPA, zasidrani z glikozil fosfatidilinozitolom, uravnavajo adhezijo, migracijo, proliferacijo in diferenciacijo z aktiviranjem določenih znotrajceličnih signalnih poti, kot sledi: signalne poti fosfatidilinozitol 4,5-difosfat 3-kinaze/Akt in ERK1/2, ki jih je mogoče preživeti, in adhezijske kinaze (FAK).
V kontekstu celjenja ran MSC je fibrinolitični faktor dokazal svoj nadaljnji pomen.Na primer, miši s pomanjkanjem plazminogena so pokazale resno zamudo pri celjenju ran, kar kaže, da je bil plazmin pomemben v tem procesu.Pri ljudeh lahko izguba plazmina povzroči tudi zaplete pri celjenju ran.Prekinitev krvnega pretoka lahko bistveno zavira regeneracijo tkiva, kar tudi pojasnjuje, zakaj so ti procesi regeneracije pri bolnikih s sladkorno boleznijo zahtevnejši.
Za pospešitev celjenja ran so na mesto rane pridobili mezenhimske matične celice kostnega mozga.V stabilnih pogojih so te celice izražale uPAuPAR in PAI-1.Zadnja dva proteina sta dejavnika, ki povzročata hipoksijo α (HIF-1 α). Ciljanje je zelo priročno, ker je HIF-1 v MSC α. Aktivacija FGF-2 in HGF je spodbudila regulacijo FGF-2 in HGF;HIF-2 α pa je VEGF-A [77] reguliran navzgor, kar skupaj prispeva k celjenju ran.Poleg tega se zdi, da HGF na sinergističen način poveča rekrutacijo mezenhimskih matičnih celic kostnega mozga v mesta rane.Opozoriti je treba, da se je izkazalo, da ishemična in hipoksična stanja znatno motijo celjenje ran.Čeprav BMSC običajno živijo v tkivih, ki zagotavljajo nizke ravni kisika, postane preživetje presajenih BMSC in vivo omejeno, ker presajene celice pogosto umrejo v neugodnih pogojih, opaženih v poškodovanih tkivih.Usoda adhezije in preživetja mezenhimskih matičnih celic kostnega mozga pod hipoksijo je odvisna od fibrinolitičnih faktorjev, ki jih izločajo te celice.PAI-1 ima visoko afiniteto za vitelin, zato lahko tekmuje za vezavo uPAR in integrina na vitelin, s čimer zavira celično adhezijo in migracijo.
Monocitni in regeneracijski sistem
Glede na literaturo obstaja veliko razprav o vlogi monocitov pri celjenju ran.Makrofagi večinoma prihajajo iz krvnih monocitov in igrajo pomembno vlogo v regenerativni medicini [81].Ker nevtrofilci izločajo IL-4, IL-1, IL-6 in TNF-α, te celice običajno prodrejo v rano približno 24-48 ur po poškodbi.Trombociti sproščajo trombin in trombocitni faktor 4 (PF4), ki lahko spodbujata pridobivanje monocitov in diferenciacijo v makrofage in dendritične celice.Pomembna značilnost makrofagov je njihova plastičnost, kar pomeni, da lahko pretvorijo fenotipe in se diferencirajo v druge vrste celic, kot so endotelijske celice, nato pa pokažejo različne funkcije različnim biokemičnim dražljajem v mikrookolju rane.Vnetne celice izražajo dva glavna fenotipa, M1 ali M2, odvisno od lokalnega molekularnega signala kot vira stimulacije.Makrofage M1 inducirajo mikrobi, zato imajo bolj vnetne učinke.V nasprotju s tem se makrofagi M2 običajno proizvajajo z reakcijami tipa 2 in imajo protivnetne lastnosti, za katere je običajno značilno povečanje IL-4, IL-5, IL-9 in IL-13.Vključen je tudi v obnavljanje tkiv s proizvodnjo rastnih faktorjev.Prehod iz podtipa M1 v M2 je v veliki meri posledica pozne faze celjenja ran.Makrofagi M1 sprožijo apoptozo nevtrofilcev in sprožijo očistek teh celic).Fagocitoza nevtrofilcev aktivira vrsto dogodkov, v katerih se izklopi proizvodnja citokinov, polarizira makrofage in sprošča TGF- β 1。 Ta rastni faktor je ključni regulator diferenciacije miofibroblastov in krčenja rane, kar omogoča razrešitev vnetja in začetek faze proliferacije v kaskadi zdravljenja [57].Druga zelo sorodna beljakovina, vključena v celične procese, je serin (SG).Ugotovljeno je bilo, da je ta hemopoetski celični sekretorni granularni proteoglikan potreben za shranjevanje sekretornih proteinov v specifičnih imunskih celicah, kot so mastociti, nevtrofilci in citotoksični T limfociti.Čeprav številne nehematopoetske celice sintetizirajo tudi plazminogen, vse vnetne celice proizvedejo veliko količino tega proteina in ga shranijo v granule za nadaljnjo interakcijo z drugimi vnetnimi mediatorji, vključno s proteazami, citokini, kemokini in rastnimi faktorji.Zdi se, da so negativno nabite glikozaminoglikanske (GAG) verige v SG kritične za stabilnost sekretornih zrnc, saj se lahko vežejo na in olajšajo shranjevanje bistveno nabitih zrnatih komponent v celici, beljakovini in verigi GAG na specifičen način.V zvezi z njihovim sodelovanjem v raziskavah PRP so Woulfe in sodelavci predhodno pokazali, da je pomanjkanje SG tesno povezano z morfološkimi spremembami trombocitov;Trombocitni faktor 4 β- Napake shranjevanja PDGF v tromboglobulinu in trombocitih;Slaba agregacija in izločanje trombocitov in vitro ter trombozna napaka in vivo.Raziskovalci so zato zaključili, da je ta proteoglikan glavni regulator tromboze.
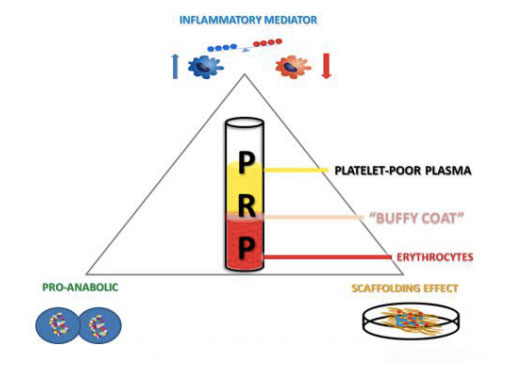
Izdelki, bogati s trombociti, lahko pridobijo osebno polno kri z zbiranjem in centrifugiranjem ter mešanico razdelijo na različne plasti, ki vsebujejo plazmo, trombocite, bele krvne celice in bele krvne celice.Ko je koncentracija trombocitov višja od osnovne vrednosti, lahko pospeši rast kosti in mehkih tkiv, z najmanj stranskimi učinki.Uporaba avtolognih PRP produktov je razmeroma nova biotehnologija, ki vseskozi kaže optimistične rezultate pri spodbujanju in pospeševanju celjenja različnih poškodb tkiv.Učinkovitost te alternativne metode zdravljenja je mogoče pripisati lokalni dostavi širokega nabora rastnih faktorjev in beljakovin za simulacijo in podporo fiziološkega celjenja ran in procesa obnove tkiva.Poleg tega ima fibrinolitični sistem očitno pomemben vpliv na celotno obnovo tkiva.Poleg spreminjanja rekrutiranja vnetnih celic in mezenhimskih matičnih celic kostnega mozga lahko uravnava tudi proteolitično aktivnost območij celjenja ran in proces regeneracije mezodermalnih tkiv, vključno s kostmi, hrustancem in mišicami, zato je ključna sestavina mišično-skeletna medicina.
Pospešeno zdravljenje je cilj, ki si ga zelo prizadevajo številni strokovnjaki na medicinskem področju.PRP predstavlja pozitivno biološko orodje, ki še naprej zagotavlja obetaven razvoj pri spodbujanju in usklajevanju kaskade regenerativnih dogodkov.Ker pa je to terapevtsko orodje še vedno zelo kompleksno, predvsem zato, ker sprošča nešteto bioaktivnih dejavnikov in njihove različne mehanizme medsebojnega delovanja ter učinke prenosa signala, so potrebne nadaljnje raziskave.
(Vsebina tega članka je ponatisnjena in ne zagotavljamo nobenega izrecnega ali implicitnega jamstva za točnost, zanesljivost ali popolnost vsebine v tem članku in nismo odgovorni za mnenja tega članka, prosimo za razumevanje.)
Čas objave: 16. december 2022